रासायनिक समीकरण कसे समान करावे हे शोधण्यासाठी, आपल्याला प्रथम या विज्ञानाचा उद्देश माहित असणे आवश्यक आहे.
व्याख्या
रसायनशास्त्र पदार्थ, त्यांचे गुणधर्म आणि परिवर्तनांचा अभ्यास करते. जर रंग, पर्जन्य, वायू पदार्थ सोडण्यात कोणताही बदल झाला नाही तर रासायनिक परस्परसंवाद होत नाही.
उदाहरणार्थ, फाईलसह लोखंडी खिळे भरताना, धातू फक्त पावडरमध्ये बदलते. या प्रकरणात, कोणतीही रासायनिक प्रतिक्रिया उद्भवत नाही.
पोटॅशियम परमॅंगनेटचे कॅलसिनेशन मॅंगनीज ऑक्साईड (4) च्या निर्मितीसह आहे, ऑक्सिजन सोडणे, म्हणजेच एक परस्परसंवाद दिसून येतो. या प्रकरणात, एक पूर्णपणे नैसर्गिक प्रश्न उद्भवतो की रासायनिक समीकरणे योग्यरित्या कशी जुळवायची. आम्ही अशा प्रक्रियेशी संबंधित सर्व सूक्ष्म गोष्टींचे विश्लेषण करू.

रासायनिक परिवर्तनांची विशिष्टता
पदार्थांच्या गुणात्मक आणि परिमाणवाचक रचनेतील बदलांसह कोणतीही घटना म्हणजे रासायनिक परिवर्तन. आण्विक स्वरूपात, वातावरणातील लोहाच्या ज्वलनाची प्रक्रिया चिन्हे आणि चिन्हे वापरून व्यक्त केली जाऊ शकते.
गुणांक ठेवण्याची पद्धत
रासायनिक समीकरणांमध्ये गुणांक कसे समान करावे? रसायनशास्त्राच्या अभ्यासक्रमात हायस्कूलइलेक्ट्रॉनिक बॅलन्सची पद्धत समजते. चला प्रक्रियेचा अधिक तपशीलवार विचार करूया. सुरुवातीस, प्रारंभिक प्रतिक्रियेमध्ये, प्रत्येकासाठी ऑक्सिडेशन अवस्थांची व्यवस्था करणे आवश्यक आहे रासायनिक घटक.
काही नियम आहेत ज्याद्वारे ते प्रत्येक घटकासाठी निर्धारित केले जाऊ शकतात. साध्या पदार्थांमध्ये, ऑक्सिडेशन अवस्था शून्य असेल. बायनरी यौगिकांमध्ये, पहिल्या घटकाचे सकारात्मक मूल्य असते, जे सर्वोच्च व्हॅलेन्सीशी संबंधित असते. नंतरचे, हे पॅरामीटर आठ मधून गट क्रमांक वजा करून निर्धारित केले जाते आणि त्यात वजा चिन्ह आहे. ऑक्सिडेशन अवस्था मोजण्यासाठी तीन घटकांचा समावेश असलेल्या सूत्रांचे स्वतःचे बारकावे आहेत.
पहिल्या आणि शेवटच्या घटकासाठी, क्रम हा बायनरी संयुगेमधील व्याख्येसारखाच असतो आणि मध्यवर्ती घटकाची गणना करण्यासाठी एक समीकरण तयार केले जाते. सर्व निर्देशकांची बेरीज शून्य इतकी असणे आवश्यक आहे, यावर आधारित, सूत्राच्या मधल्या घटकासाठी निर्देशकाची गणना केली जाते.
इलेक्ट्रॉन बॅलन्स पद्धतीचा वापर करून रासायनिक समीकरणे कशी समान करायची याबद्दल संभाषण सुरू ठेवूया. ऑक्सिडेशन स्थिती सेट केल्यानंतर, ते आयन किंवा पदार्थ निर्धारित करणे शक्य आहे ज्यांनी रासायनिक परस्परसंवाद दरम्यान त्यांचे मूल्य बदलले आहे.
अधिक आणि वजा चिन्हे रासायनिक परस्परसंवादाच्या प्रक्रियेत स्वीकारलेल्या (दिलेल्या) इलेक्ट्रॉनची संख्या दर्शवतात. मिळालेल्या संख्यांमध्ये, किमान सामान्य गुणाकार शोधा.
प्राप्त आणि दिलेल्या इलेक्ट्रॉनमध्ये विभागताना, गुणांक प्राप्त होतात. रासायनिक समीकरण कसे संतुलित करावे? ताळेबंदात मिळालेले आकडे संबंधित सूत्रांसमोर ठेवले पाहिजेत. डाव्या आणि उजव्या भागांमधील प्रत्येक घटकाची संख्या तपासणे ही एक पूर्व शर्त आहे. गुणांक योग्यरित्या ठेवले असल्यास, त्यांची संख्या समान असावी.

पदार्थांच्या वस्तुमानाच्या संवर्धनाचा कायदा
रासायनिक समीकरण कसे समान करायचे यावर वाद घालताना या कायद्याचा वापर करणे आवश्यक आहे. रासायनिक अभिक्रियामध्ये प्रवेश केलेल्या पदार्थांचे वस्तुमान परिणामी उत्पादनांच्या वस्तुमानाच्या बरोबरीचे आहे हे लक्षात घेता, सूत्रांसमोर गुणांक सेट करणे शक्य होते. उदाहरणार्थ, जर साधे पदार्थ कॅल्शियम आणि ऑक्सिजन परस्परसंवाद करतात आणि प्रक्रिया पूर्ण झाल्यानंतर, ऑक्साईड प्राप्त झाल्यास रासायनिक समीकरण कसे जुळवायचे?
कार्याचा सामना करण्यासाठी, हे लक्षात घेतले पाहिजे की ऑक्सिजन हे सहसंयोजक नॉन-ध्रुवीय बंध असलेले डायटॉमिक रेणू आहे, म्हणून त्याचे सूत्र खालील स्वरूपात लिहिलेले आहे - O2. उजव्या बाजूला, कॅल्शियम ऑक्साईड (CaO) संकलित करताना, प्रत्येक घटकाची व्हॅलेन्सी विचारात घेतली जाते.
प्रथम आपल्याला समीकरणाच्या प्रत्येक भागामध्ये ऑक्सिजनचे प्रमाण तपासण्याची आवश्यकता आहे, कारण ते भिन्न आहे. पदार्थांच्या वस्तुमानाच्या संवर्धनाच्या कायद्यानुसार, उत्पादनाच्या सूत्रासमोर 2 चा घटक ठेवणे आवश्यक आहे. पुढे, कॅल्शियम तपासले जाते. ते समान करण्यासाठी, आम्ही मूळ पदार्थासमोर 2 चा घटक ठेवतो. परिणामी, आम्हाला रेकॉर्ड मिळते:
- 2Ca+O2=2CaO.

इलेक्ट्रॉनिक शिल्लक पद्धतीद्वारे प्रतिक्रियेचे विश्लेषण
रासायनिक समीकरणे कशी जुळवायची? RIA ची उदाहरणे या प्रश्नाचे उत्तर देण्यास मदत करतील. समजा की इलेक्ट्रॉनिक शिल्लक पद्धत वापरून प्रस्तावित योजनेमध्ये गुणांक ठेवणे आवश्यक आहे:
- CuO + H2=Cu + H2O.
सुरुवातीला, प्रारंभिक पदार्थ आणि परस्परसंवाद उत्पादनांमधील प्रत्येक घटकासाठी, आम्ही ऑक्सिडेशन स्थितींची मूल्ये ठेवू. मिळवा पुढील दृश्यसमीकरणे:
- Cu(+2)O(-2)+H2(0)=Cu(0)+H2(+)O(-2).
तांबे आणि हायड्रोजनसाठी निर्देशक बदलले आहेत. त्यांच्या आधारावर आम्ही इलेक्ट्रॉनिक शिल्लक काढू:
- Cu(+2)+2e=Cu(0) 1 कमी करणारा घटक, ऑक्सिडेशन;
- H2(0)-2e=2H(+) 1 ऑक्सिडायझिंग एजंट, घट.
इलेक्ट्रॉनिक बॅलन्समध्ये मिळालेल्या गुणांकांच्या आधारे, आम्ही प्रस्तावित रासायनिक समीकरणाचा खालील रेकॉर्ड मिळवतो:
- CuO+H2=Cu+H2O.
चला आणखी एक उदाहरण घेऊ ज्यामध्ये गुणांक सेट करणे समाविष्ट आहे:
- H2+O2=H2O.
पदार्थांच्या संवर्धनाच्या कायद्याच्या आधारे ही योजना समान करण्यासाठी, ऑक्सिजनपासून सुरुवात करणे आवश्यक आहे. प्रतिक्रियेमध्ये डायटॉमिक रेणू प्रवेश केला हे लक्षात घेता, परस्परसंवाद उत्पादनाच्या सूत्रापूर्वी 2 चा घटक ठेवणे आवश्यक आहे.
- 2H2+O2=2H2O.

निष्कर्ष
इलेक्ट्रॉनिक बॅलन्सवर आधारित, तुम्ही कोणत्याही रासायनिक समीकरणांमध्ये गुणांक ठेवू शकता. नववी आणि अकरावीचे पदवीधर शैक्षणिक संस्था, रसायनशास्त्रातील परीक्षा निवडताना, अंतिम चाचण्यांपैकी एका कार्यात ते समान कार्ये देतात.
रेडॉक्स प्रतिक्रियांच्या समीकरणांमध्ये गुणांक निश्चित करण्यासाठी अनेक पद्धती आहेत. आम्ही इलेक्ट्रॉनिक शिल्लक पद्धत वापरतो, ज्यामध्ये संपूर्ण OVR समीकरणाचे संकलन खालील क्रमाने केले जाते:
1. प्रतिक्रिया देणारे पदार्थ आणि प्रतिक्रियेमुळे निर्माण होणारे पदार्थ दर्शवणारी प्रतिक्रिया योजना तयार करा, उदाहरणार्थ:
2. अणूंची ऑक्सिडेशन स्थिती निश्चित करा आणि त्याचे चिन्ह आणि मूल्य घटकांच्या चिन्हाच्या वर लिहा, ज्या घटकांची ऑक्सिडेशन स्थिती बदलली आहे ते चिन्हांकित करा:
3. ऑक्सिडेशन आणि रिडक्शन रिअॅक्शन्सची इलेक्ट्रॉनिक समीकरणे लिहा, कमी करणार्या एजंटने दान केलेल्या आणि ऑक्सिडायझिंग एजंटने स्वीकारलेल्या इलेक्ट्रॉनची संख्या निर्धारित करा आणि नंतर त्यांना योग्य गुणांकाने गुणाकार करून समान करा:
4. इलेक्ट्रॉनिक शिल्लकशी संबंधित प्राप्त गुणांक मुख्य समीकरणामध्ये हस्तांतरित केले जातात:
5. ऑक्सिडेशनची डिग्री बदलत नसलेल्या अणू आणि आयनांची संख्या समान करा (क्रमात: धातू, नॉन-मेटल्स, हायड्रोजन):
6. प्रतिक्रिया समीकरणाच्या डाव्या आणि उजव्या भागांमधील ऑक्सिजन अणूंच्या संख्येनुसार गुणांकांच्या निवडीची शुद्धता तपासा - ते समान असले पाहिजेत (या समीकरणात 24 = 18 + 2 + 4, 24 = 24).
चला अधिक जटिल उदाहरण पाहू:
रेणूंमधील अणूंच्या ऑक्सिडेशन अवस्था निश्चित करूया:
आम्ही ऑक्सिडेशन आणि रिडक्शनच्या प्रतिक्रियांसाठी इलेक्ट्रॉनिक समीकरणे तयार करतो आणि दिलेल्या आणि प्राप्त झालेल्या इलेक्ट्रॉनच्या संख्येची समानता करतो:
मुख्य समीकरणात गुणांक हस्तांतरित करू:
ऑक्सिडेशन स्थिती बदलत नसलेल्या अणूंची संख्या समान करा:
समीकरणाच्या उजव्या आणि डाव्या बाजूला ऑक्सिजन अणूंची संख्या मोजून, आम्ही गुणांक योग्यरित्या निवडले आहेत याची खात्री करतो.
सर्वात महत्वाचे ऑक्सिडायझिंग आणि कमी करणारे एजंट
घटकांचे रेडॉक्स गुणधर्म अणूंच्या इलेक्ट्रॉन शेलच्या संरचनेवर अवलंबून असतात आणि मेंडेलीव्हच्या नियतकालिक प्रणालीमध्ये त्यांच्या स्थितीनुसार निर्धारित केले जातात.
बाह्य उर्जेच्या पातळीवर 1-3 इलेक्ट्रॉन असलेले धातू, त्यांना सहजतेने सोडून देतात आणि केवळ कमी करणारे गुणधर्म दर्शवतात. धातू नसलेले (गट IV-VII चे घटक) इलेक्ट्रॉन दान आणि स्वीकारू शकतात, त्यामुळे ते कमी करणारे आणि ऑक्सिडायझिंग गुणधर्म दोन्ही प्रदर्शित करू शकतात. घटकांच्या क्रमिक संख्येत वाढ होण्याच्या कालावधीत, साध्या पदार्थांचे कमी करणारे गुणधर्म कमकुवत होतात आणि ऑक्सिडायझिंग वाढतात. अनुक्रमांक वाढलेल्या गटांमध्ये, कमी करणारे गुणधर्म वर्धित केले जातात आणि ऑक्सिडेटिव्ह गुणधर्म कमकुवत होतात. अशा प्रकारे, साध्या पदार्थांचे, सर्वोत्तम कमी करणारे एजंट आहेत अल्कली धातू, अॅल्युमिनियम, हायड्रोजन, कार्बन; सर्वोत्तम ऑक्सिडायझिंग एजंट हॅलोजन आणि ऑक्सिजन आहेत.
जटिल पदार्थांचे रेडॉक्स गुणधर्म त्यांची रचना बनवणाऱ्या अणूंच्या ऑक्सिडेशनच्या डिग्रीवर अवलंबून असतात. सर्वात कमी ऑक्सिडेशन स्थिती असलेले अणू असलेले पदार्थ कमी करणारे गुणधर्म प्रदर्शित करतात. सर्वात महत्वाचे कमी करणारे एजंट कार्बन मोनोऑक्साइड आहेत.  , हायड्रोजन सल्फाइड
, हायड्रोजन सल्फाइड  , लोह(II) सल्फेट
, लोह(II) सल्फेट  .सर्वाधिक ऑक्सिडेशन अवस्थेसह अणू असलेले पदार्थ ऑक्सिडायझिंग गुणधर्म प्रदर्शित करतात. पोटॅशियम परमॅंगनेट हे सर्वात महत्वाचे ऑक्सिडायझिंग एजंट आहेत
.सर्वाधिक ऑक्सिडेशन अवस्थेसह अणू असलेले पदार्थ ऑक्सिडायझिंग गुणधर्म प्रदर्शित करतात. पोटॅशियम परमॅंगनेट हे सर्वात महत्वाचे ऑक्सिडायझिंग एजंट आहेत  , पोटॅशियम डायक्रोमेट
, पोटॅशियम डायक्रोमेट  , हायड्रोजन पेरोक्साइड
, हायड्रोजन पेरोक्साइड  , नायट्रिक आम्ल
, नायट्रिक आम्ल  , केंद्रित सल्फ्यूरिक ऍसिड
, केंद्रित सल्फ्यूरिक ऍसिड  .
.
मध्यवर्ती ऑक्सिडेशन स्थिती असलेले अणू असलेले पदार्थ ऑक्सिडायझिंग किंवा कमी करणारे एजंट म्हणून वागू शकतात.ज्या पदार्थांशी ते संवाद साधतात त्यांच्या गुणधर्मांवर आणि प्रतिक्रियेच्या परिस्थितीवर अवलंबून. त्यामुळे प्रतिक्रियेत  सल्फ्यूरिक ऍसिड कमी करणारे गुणधर्म प्रदर्शित करते:
सल्फ्यूरिक ऍसिड कमी करणारे गुणधर्म प्रदर्शित करते:
आणि हायड्रोजन सल्फाइडशी संवाद साधताना, ते ऑक्सिडायझिंग एजंट आहे:

याव्यतिरिक्त, अशा पदार्थांसाठी, सेल्फ-ऑक्सिडेशन-स्व-पुनर्प्राप्ती प्रतिक्रिया शक्य आहेत, त्याच घटकाच्या अणूंच्या ऑक्सिडेशनच्या डिग्रीमध्ये एकाच वेळी वाढ आणि घट झाल्यामुळे, उदाहरणार्थ:
अनेक ऑक्सिडायझिंग आणि रिड्यूसिंग एजंट्सची ताकद माध्यमाच्या pH वर अवलंबून असते. उदाहरणार्थ, 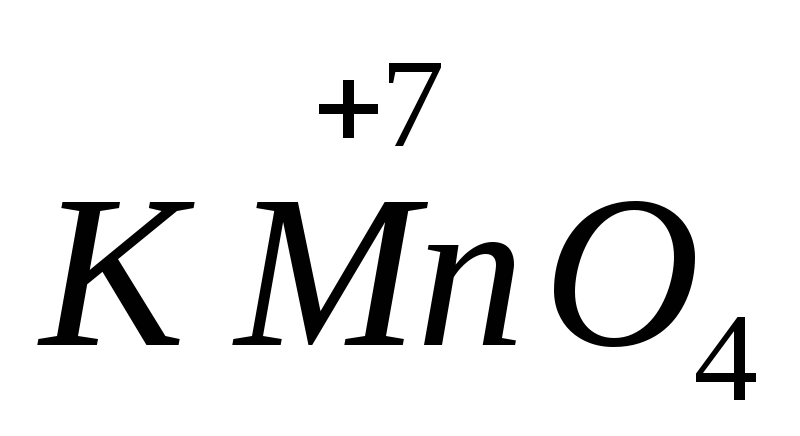 क्षारीय वातावरणात कमी होते
क्षारीय वातावरणात कमी होते  , तटस्थ मध्ये
, तटस्थ मध्ये  , सल्फ्यूरिक ऍसिडच्या उपस्थितीत - पर्यंत
, सल्फ्यूरिक ऍसिडच्या उपस्थितीत - पर्यंत  .
.
एल  रासायनिक समीकरणांमध्ये गुणांकांची मांडणी करणे सोपे आहे का?
रासायनिक समीकरणांमध्ये गुणांकांची मांडणी करणे सोपे आहे का?
येथे माझी मुले आहेत आणि ते रसायनशास्त्रात मोठे झाले आहेत (मी 8 व्या "ब" वर्गात वर्ग शिक्षक आहे). रसायनशास्त्र बहुतेकदा मुलांना पहिल्या धड्यात दिले जाते, परंतु गुरुवारी माझ्याकडे पहिला धडा नाही आणि मी व्हॅलेंटिना इव्हानोव्हना यांच्याकडे “मुलांकडे पाहण्यासाठी” आणि डायरी तपासण्यासाठी धडा मागितला. या विषयाने मला आकर्षित केले, शाळेत मला रसायनशास्त्र आवडले आणि मी डायरी तपासली नाही. पुन्हा एकदा, मला खात्री पटली की विद्यार्थ्यांना आंतरविद्याशाखीय कनेक्शन दिसत नसल्यामुळे बहुतेकदा अडचणी येतात. या रसायनशास्त्राच्या धड्यात विद्यार्थ्यांना रसायनांची व्हॅलेन्सी जाणून घेऊन रासायनिक समीकरणे लिहायची होती. आणि अनेक विद्यार्थ्यांना संख्यात्मक गुणांक ठरवण्यात अडचण आली. शनिवारी पुढील रसायनशास्त्राचा धडा व्हॅलेंटिना इव्हानोव्हनासोबत घालवला.
व्यायाम १.
खालील वाक्ये रासायनिक समीकरणांच्या स्वरूपात लिहा:
अ) "कॅल्शियम कार्बोनेटच्या फायरिंग दरम्यान, कॅल्शियम ऑक्साईड आणि कार्बन मोनोऑक्साइड (IV) तयार होतात"; b) "जेव्हा फॉस्फरस (V) ऑक्साईडची पाण्याशी प्रतिक्रिया होते तेव्हा फॉस्फोरिक ऍसिड मिळते."
निर्णय:
अ) CaCO 3 \u003d CaO + CO 2 - प्रतिक्रिया एंडोथर्मिक आहे. या कार्यात कोणतीही अडचण नव्हती, कारण संख्यात्मक गुणांक शोधणे आवश्यक नव्हते. सुरुवातीला, समानतेच्या डाव्या आणि उजव्या भागांमध्ये, प्रत्येकी एक कॅल्शियम अणू, एक कार्बन अणू आणि तीन ऑक्सिजन अणू असतात.
ब) P 2 O 5 + 3H 2 O \u003d 2H 3 PO 4 - प्रतिक्रिया एक्झोथर्मिक आहे. दुसऱ्या समीकरणात समस्या उद्भवल्या, संख्यात्मक गुणांकांशिवाय योग्य समानता निघाली नाही: P 2 O 5 + H 2 O → H 3 PO 4. अर्थात, योग्य समानता संकलित करण्यासाठी, आपल्याला संख्यात्मक गुणांक निवडण्याची आवश्यकता आहे. आपण निवडल्यास, आपण फॉस्फरससह प्रारंभ करू शकता: डावीकडे दोन अणू आहेत आणि एक उजवीकडे आहे, म्हणून आम्ही नायट्रिक ऍसिड सूत्रासमोर दोन समान संख्यात्मक घटक ठेवतो आणि नंतर आम्हाला मिळते: P 2 O 5 + H 2 O → 2H 3 PO 4. परंतु आता ऑक्सिजन आणि हायड्रोजन अणूंची संख्या समान करणे बाकी आहे: डाव्या बाजूला दोन हायड्रोजन अणू आहेत आणि उजवीकडे सहा अणू आहेत, म्हणून आम्ही पाण्याच्या सूत्रासमोर तीन समान संख्यात्मक गुणांक ठेवतो आणि नंतर आम्हाला मिळते: P 2 O 5 + 3H 2 O → 2H 3 PO 4. आता हे सुनिश्चित करणे सोपे आहे की समीकरणाच्या प्रत्येक भागात फॉस्फरस अणू आणि हायड्रोजन अणू आणि ऑक्सिजन अणू समान प्रमाणात आहेत, म्हणून, आम्हाला योग्य रासायनिक अभिक्रिया समीकरण प्राप्त झाले आहे: P 2 O 5 + 3H 2 O \u003d 2H 3 PO 4.
दुसरा मार्ग: बीजगणितआपण समीकरणात तीन गुणांक ठेवतो असे गृहीत धरू a, b, c , परिणामी योग्य रासायनिक अभिक्रिया समीकरण: a P2O5+ मध्ये H 2 O = सह H3PO4. समीकरण अणू वापरत असल्याने तीन प्रकार, नंतर आम्ही तीन प्रणाली बनवतो रेखीय समीकरणेतीन अज्ञातांसह a, मध्येआणि सह .
रासायनिक अभिक्रियामध्ये वापरलेले पदार्थ: पी - फॉस्फरस; ओ 2 - ऑक्सिजन; P 2 O 5 - फॉस्फरस ऑक्साईड (V).
C) Fe 2 (SO 4) 3 + KOH → Fe (OH) 3 + K 2 SO 4.
रासायनिक अभिक्रियामध्ये वापरलेले पदार्थ: Fe 2 (SO 4) 3 - लोह सल्फेट (III); KOH, पोटॅशियम हायड्रॉक्साइड; Fe (OH) 3 - लोह (III) हायड्रॉक्साइड; K 2 SO 4 - पोटॅशियम सल्फेट.
ड) CuOH → Cu 2 O + H 2 O.
निर्णय: 2CuOH \u003d Cu 2 O + H 2 O. संख्यात्मक गुणांक ठरवण्याची समस्या समीकरणांची प्रणाली संकलित करून सोडवली गेली: 
रासायनिक अभिक्रियामध्ये वापरलेले पदार्थ: CuOH - तांबे (I) हायड्रॉक्साइड; Cu 2 O - तांबे (I) ऑक्साईड; H 2 O - पाणी.
ई) CS 2 + O 2 → CO 2 + SO 2.
निर्णय: CS 2 + 3O 2 \u003d CO 2 + 2SO 2. गुणांकांच्या निवडीद्वारे निर्णय घेतला: सल्फर अणूंची संख्या समान केली (2); ऑक्सिजन अणूंची संख्या समान केली (3).
रासायनिक अभिक्रियामध्ये वापरलेले पदार्थ: CS 2 - सल्फर सल्फाइड (IV); O2-
रासायनिक अभिक्रियामध्ये वापरलेले पदार्थ: FeS 2 - पायराइट्स; ओ 2 - ऑक्सिजन; Fe 2 O 3 - लोह ऑक्साईड (III); SO 2 - सल्फर ऑक्साईड (IV).
व्यायाम 3
(म्हणून समाधानासाठी सुचवले आहे स्वतंत्र काम).
अट:
समीकरणे लिहा रासायनिक प्रतिक्रियाखालील योजनांनुसार:
अ) फॉस्फोरिक ऍसिड + सोडियम हायड्रॉक्साइड → सोडियम फॉस्फेट + पाणी;
ब) सोडियम ऑक्साईड + पाणी → सोडियम हायड्रॉक्साईड;
क) लोह ऑक्साईड (II) + अॅल्युमिनियम → अॅल्युमिनियम ऑक्साईड + लोह;
ड) तांबे (II) हायड्रॉक्साइड → तांबे (II) ऑक्साइड + पाणी.
उत्तर:
अ) 2H 3 PO 4 + 6NaOH \u003d 2Na 3 PO 4 + 6H 2 O;
ब) Na 2 O + H 2 O \u003d 2NaOH;
क) 3FeO + 2Al = Al 2 O 3 + 3Fe;
ड) Cu (OH) 2 \u003d CuO + H 2 O.
10 मिनिटांत, 85% विद्यार्थ्यांनी उत्कृष्ट गुणांसह कार्य पूर्ण केले, ज्यामुळे व्हॅलेंटिना इव्हानोव्हना आनंदाने आश्चर्यचकित झाले.
1. एक प्रतिक्रिया योजना बनवूया:
धड्याची उद्दिष्टे.शैक्षणिक.रेडॉक्स प्रतिक्रिया (ORD) सह घटकांच्या ऑक्सिडेशन स्थितीतील बदलांच्या आधारे रासायनिक अभिक्रियांच्या नवीन वर्गीकरणासह विद्यार्थ्यांना परिचित करण्यासाठी; विद्यार्थ्यांना इलेक्ट्रॉनिक शिल्लक पद्धत वापरून गुणांकांची मांडणी करण्यास शिकवा.
विकसनशील.विकास सुरू ठेवा तार्किक विचार, विश्लेषण आणि तुलना करण्याची क्षमता, विषयात स्वारस्य निर्माण करणे.
शैक्षणिक.विद्यार्थ्यांचे वैज्ञानिक जागतिक दृष्टिकोन तयार करण्यासाठी; कामाची कौशल्ये सुधारणे.
पद्धती आणि पद्धतशीर तंत्रे.कथा, संभाषण, व्हिज्युअल एड्सचे प्रात्यक्षिक, विद्यार्थ्यांचे स्वतंत्र कार्य.
उपकरणे आणि अभिकर्मक.कोलोसस ऑफ रोड्सचे चित्रण करणारे पुनरुत्पादन, इलेक्ट्रॉनिक शिल्लक पद्धतीनुसार गुणांक ठेवण्यासाठी अल्गोरिदम, ठराविक ऑक्सिडायझिंग आणि रिड्यूसिंग एजंट्सची टेबल, एक क्रॉसवर्ड कोडे; Fe (नखे), NaOH, CuSO4 चे उपाय.
वर्ग दरम्यान
परिचय
(प्रेरणा आणि ध्येय सेटिंग)
शिक्षक. तिसऱ्या शतकात. इ.स.पू. रोड्स बेटावर, हेलिओस (ग्रीक लोकांमध्ये - सूर्याचा देव) च्या विशाल पुतळ्याच्या रूपात एक स्मारक बांधले गेले. कोलोसस ऑफ रोड्सच्या अंमलबजावणीची भव्य कल्पना आणि परिपूर्णता - जगातील आश्चर्यांपैकी एक - ज्यांनी ते पाहिले त्या सर्वांना आश्चर्यचकित केले.
हा पुतळा नेमका कसा दिसत होता हे आम्हाला माहित नाही, परंतु हे माहित आहे की ती कांस्य बनलेली होती आणि सुमारे 33 मीटर उंचीवर पोहोचली होती. ही मूर्ती शिल्पकार हारेट यांनी तयार केली होती आणि तयार करण्यासाठी 12 वर्षे लागली.
पितळेचे कवच लोखंडी चौकटीला जोडलेले होते. पोकळ पुतळा तळापासून बांधला जाऊ लागला आणि जसजसा तो वाढत गेला तसतसा तो अधिक स्थिर करण्यासाठी दगडांनी भरला गेला. बांधकाम पूर्ण झाल्यानंतर सुमारे 50 वर्षांनी कोलोसस कोसळला. भूकंपाच्या वेळी तो त्याच्या गुडघ्याच्या पातळीवर तुटला.
शास्त्रज्ञांचा असा विश्वास आहे की या चमत्काराच्या नाजूकपणाचे खरे कारण धातूचा गंज होता. आणि गंज प्रक्रियेच्या केंद्रस्थानी रेडॉक्स प्रतिक्रिया असतात.
आज धड्यात तुम्ही रेडॉक्स प्रतिक्रियांशी परिचित व्हाल; "रिड्यूसिंग एजंट" आणि "ऑक्सिडायझिंग एजंट" च्या संकल्पना, घट आणि ऑक्सिडेशनच्या प्रक्रियेबद्दल जाणून घ्या; रेडॉक्स प्रतिक्रियांच्या समीकरणांमध्ये गुणांक कसे व्यवस्थित करायचे ते शिका. तुमच्या वर्कबुकमध्ये धड्याचा विषय, संख्या लिहा.
नवीन साहित्य शिकणे
शिक्षक दोन प्रात्यक्षिक प्रयोग करतात: तांबे (II) सल्फेटचा अल्कलीशी परस्परसंवाद आणि त्याच मीठाचा लोहासह परस्परसंवाद.
शिक्षक. केलेल्या प्रतिक्रियांची आण्विक समीकरणे लिहा. प्रत्येक समीकरणामध्ये, प्रारंभिक सामग्री आणि प्रतिक्रिया उत्पादनांच्या सूत्रांमध्ये घटकांच्या ऑक्सिडेशन स्थितीची मांडणी करा.
विद्यार्थी फलकावर प्रतिक्रिया समीकरणे लिहितो आणि ऑक्सिडेशन अवस्थांची मांडणी करतो:
शिक्षक. या प्रतिक्रियांमध्ये घटकांच्या ऑक्सिडेशन अवस्था बदलल्या आहेत का?
विद्यार्थी. पहिल्या समीकरणात, घटकांच्या ऑक्सिडेशन स्थिती बदलल्या नाहीत, परंतु दुसऱ्यामध्ये ते बदलले - तांबे आणि लोखंडात.
शिक्षक. दुसरी प्रतिक्रिया रेडॉक्स आहे. रेडॉक्स प्रतिक्रिया परिभाषित करण्याचा प्रयत्न करा.
विद्यार्थी. प्रतिक्रिया, ज्याच्या परिणामी अभिक्रियाक आणि प्रतिक्रिया उत्पादने बनविणाऱ्या घटकांच्या ऑक्सिडेशन अवस्था बदलतात, त्यांना रेडॉक्स प्रतिक्रिया म्हणतात.
विद्यार्थी एका नोटबुकमध्ये शिक्षकांच्या श्रुतलेखाखाली रेडॉक्स प्रतिक्रियांची व्याख्या लिहितात.
शिक्षक. रेडॉक्स प्रतिक्रियेच्या परिणामी काय झाले? प्रतिक्रियेपूर्वी, लोहाची ऑक्सीकरण स्थिती 0 होती, प्रतिक्रियेनंतर ते +2 झाले. जसे आपण पाहू शकता, ऑक्सिडेशन स्थिती वाढली आहे, म्हणून, लोह 2 इलेक्ट्रॉन सोडते.
तांब्याची ऑक्सिडेशन स्थिती प्रतिक्रियेपूर्वी +2 असते आणि प्रतिक्रियेनंतर 0 असते. तुम्ही बघू शकता, ऑक्सिडेशन स्थिती कमी झाली आहे. म्हणून, तांबे 2 इलेक्ट्रॉन स्वीकारतात.
लोह इलेक्ट्रॉन दान करते, ते कमी करणारे एजंट आहे आणि इलेक्ट्रॉन हस्तांतरणाच्या प्रक्रियेला ऑक्सिडेशन म्हणतात.
कॉपर इलेक्ट्रॉन्स स्वीकारतो, तो ऑक्सिडायझिंग एजंट आहे आणि इलेक्ट्रॉन जोडण्याच्या प्रक्रियेला घट म्हणतात.
आम्ही या प्रक्रियेच्या योजना लिहितो:
तर, "रिड्युसिंग एजंट" आणि "ऑक्सिडायझिंग एजंट" च्या संकल्पनांची व्याख्या द्या.
विद्यार्थी. अणू, रेणू किंवा आयन जे इलेक्ट्रॉन दान करतात त्यांना कमी करणारे एजंट म्हणतात.
अणू, रेणू किंवा आयन जे इलेक्ट्रॉन स्वीकारतात त्यांना ऑक्सिडायझिंग एजंट म्हणतात.
शिक्षक. घट आणि ऑक्सिडेशन प्रक्रियांची व्याख्या काय आहे?
विद्यार्थी. पुनर्प्राप्ती ही अणू, रेणू किंवा आयनमध्ये इलेक्ट्रॉन जोडण्याची प्रक्रिया आहे.
ऑक्सिडेशन ही प्रक्रिया आहे ज्याद्वारे इलेक्ट्रॉन्स अणू, रेणू किंवा आयनद्वारे हस्तांतरित केले जातात.
विद्यार्थी श्रुतलेखाखाली व्याख्या लिहितात आणि रेखाचित्र पूर्ण करतात.
लक्षात ठेवा!
इलेक्ट्रॉन दान करा - ऑक्सिडाइझ करा.
इलेक्ट्रॉन घ्या - पुनर्प्राप्त करा.
शिक्षक. ऑक्सिडेशन नेहमी कपात सह आहे, आणि उलट, कपात नेहमी ऑक्सिडेशन संबद्ध आहे. रिड्यूसिंग एजंटने दान केलेल्या इलेक्ट्रॉनची संख्या ऑक्सिडायझिंग एजंटने जोडलेल्या इलेक्ट्रॉनच्या संख्येइतकी असते.
रेडॉक्स प्रतिक्रियांच्या समीकरणांमधील गुणांक निवडण्यासाठी, दोन पद्धती वापरल्या जातात - इलेक्ट्रॉन शिल्लक आणि इलेक्ट्रॉन-आयन शिल्लक (अर्ध-प्रतिक्रिया पद्धत).
आम्ही फक्त इलेक्ट्रॉनिक शिल्लक पद्धतीचा विचार करू. हे करण्यासाठी, आम्ही इलेक्ट्रॉनिक शिल्लक पद्धत (ड्रॉइंग पेपरच्या तुकड्यावर काढलेली) वापरून गुणांकांची मांडणी करण्यासाठी अल्गोरिदम वापरतो.
उदाहरण इलेक्ट्रॉन शिल्लक पद्धतीचा वापर करून या प्रतिक्रिया योजनेतील गुणांकांची मांडणी करा, ऑक्सिडायझिंग एजंट आणि कमी करणारे एजंट निश्चित करा, ऑक्सिडेशन आणि घट करण्याच्या प्रक्रिया दर्शवा:
Fe2O3 + CO Fe + CO2.
इलेक्ट्रॉनिक शिल्लक पद्धत वापरून गुणांक ठेवण्यासाठी आम्ही अल्गोरिदम वापरू.
3. ऑक्सिडेशनची डिग्री बदलणारे घटक लिहू:
4. दिलेल्या आणि प्राप्त झालेल्या इलेक्ट्रॉनची संख्या ठरवून इलेक्ट्रॉनिक समीकरणे तयार करा:
5. दिलेल्या आणि प्राप्त झालेल्या इलेक्ट्रॉनची संख्या समान असली पाहिजे, कारण अभिक्रियाक किंवा प्रतिक्रियेच्या उत्पादनांवर शुल्क आकारले जात नाही. किमान सामान्य मल्टिपल (एलसीएम) आणि अतिरिक्त घटक निवडून आम्ही दिलेल्या आणि प्राप्त झालेल्या इलेक्ट्रॉनच्या संख्येची समानता करतो:
6. परिणामी गुणक गुणांक आहेत. आम्ही गुणांक प्रतिक्रिया योजनेमध्ये हस्तांतरित करतो:
Fe2O3 + 3CO = 2Fe + 3CO2.
जे पदार्थ अनेक प्रतिक्रियांमध्ये ऑक्सिडायझिंग किंवा कमी करणारे घटक असतात त्यांना वैशिष्ट्यपूर्ण म्हणतात.
व्हॉटमॅन शीटवर बनवलेले टेबल पोस्ट केले आहे.
शिक्षक. रेडॉक्स प्रतिक्रिया खूप सामान्य आहेत. ते केवळ गंज प्रक्रियांशीच नव्हे तर सजीवांमध्ये होणार्या किण्वन, क्षय, प्रकाशसंश्लेषण आणि चयापचय प्रक्रियांशी देखील संबंधित आहेत. ते इंधनाच्या ज्वलन दरम्यान पाहिले जाऊ शकतात.
रासायनिक समीकरण कसे समान करावे: नियम आणि अल्गोरिदम
रेडॉक्स प्रक्रिया निसर्गातील पदार्थांच्या चक्रासोबत असतात.
तुम्हाला माहित आहे का की दररोज सुमारे 2 दशलक्ष टन नायट्रिक ऍसिड वातावरणात तयार होते, किंवा
दरवर्षी 700 दशलक्ष टन, आणि कमकुवत द्रावणाच्या रूपात पावसासह जमिनीवर पडतात (मनुष्य वर्षाला फक्त 30 दशलक्ष टन नायट्रिक ऍसिड तयार करतो).
वातावरणात काय होते?
हवेमध्ये प्रमाणानुसार 78% नायट्रोजन, 21% ऑक्सिजन आणि 1% इतर वायू असतात. विजा पडण्याच्या क्रियेच्या अंतर्गत, आणि पृथ्वीवर दर सेकंदाला सरासरी 100 वीज चमकतात, नायट्रोजन रेणू ऑक्सिजन रेणूंशी संवाद साधून नायट्रिक ऑक्साईड (II):
नायट्रिक ऑक्साईड (II) हे वातावरणातील ऑक्सिजनद्वारे नायट्रिक ऑक्साईड (IV) मध्ये सहजपणे ऑक्सिडाइझ केले जाते:
परिणामी नायट्रिक ऑक्साईड (IV) ऑक्सिजनच्या उपस्थितीत वातावरणातील आर्द्रतेशी संवाद साधतो, नायट्रिक ऍसिडमध्ये बदलतो:
NO2 + H2O + O2 HNO3.
या सर्व प्रतिक्रिया रेडॉक्स प्रतिक्रिया आहेत.
कार्य . इलेक्ट्रॉनिक शिल्लक पद्धतीचा वापर करून वरील प्रतिक्रिया योजनांमधील गुणांकांची मांडणी करा, ऑक्सिडायझिंग एजंट, कमी करणारे एजंट, ऑक्सिडेशन आणि घट प्रक्रिया दर्शवा.
निर्णय
1. घटकांच्या ऑक्सिडेशन अवस्था निर्धारित करू:
2. ज्या घटकांच्या ऑक्सिडेशन स्थिती बदलतात त्यांची चिन्हे आम्ही अधोरेखित करतो:
3. ज्या घटकांनी त्यांची ऑक्सिडेशन स्थिती बदलली आहे ते लिहूया:
4. इलेक्ट्रॉनिक समीकरणे तयार करा (दिलेल्या आणि प्राप्त झालेल्या इलेक्ट्रॉनची संख्या निश्चित करा):
5. दिलेल्या आणि प्राप्त इलेक्ट्रॉन्सची संख्या समान आहे.
6. आम्ही पासून गुणांक हस्तांतरित करतो इलेक्ट्रॉनिक सर्किट्सप्रतिक्रिया योजनेत:
पुढे, विद्यार्थ्यांना इलेक्ट्रॉनिक शिल्लक पद्धतीचा वापर करून गुणांकांची स्वतंत्रपणे मांडणी करण्यासाठी, ऑक्सिडायझिंग एजंट, कमी करणारे एजंट निश्चित करण्यासाठी, ऑक्सिडेशनच्या प्रक्रिया आणि निसर्गात होणार्या इतर प्रक्रियांमध्ये घट दर्शवण्यासाठी आमंत्रित केले जाते.
इतर दोन प्रतिक्रिया समीकरणे (गुणांकांसह) आहेत:
कोडोस्कोप वापरून कार्यांची शुद्धता तपासली जाते.
शेवटचा भाग
शिक्षक विद्यार्थ्यांना अभ्यास केलेल्या साहित्यावर आधारित क्रॉसवर्ड कोडे सोडवण्यास सांगतात. कामाचा निकाल पडताळणीसाठी सादर केला जातो.
अंदाज येत शब्दकोड, तुम्हाला कळेल की KMnO4, K2Cr2O7, O3 हे पदार्थ मजबूत आहेत... (उभ्या बाजूने (2)).
क्षैतिज:
1. योजना कोणती प्रक्रिया प्रतिबिंबित करते:
3. प्रतिक्रिया
N2 (g.) + 3H2 (g.) 2NH3 (g.) + प्र
रेडॉक्स, उलट करता येण्याजोगे, एकसंध, ….
4. ... कार्बन(II) हा एक सामान्य कमी करणारा घटक आहे.
5. योजना कोणती प्रक्रिया प्रतिबिंबित करते:
6. रेडॉक्स प्रतिक्रियांच्या समीकरणांमध्ये गुणांक निवडण्यासाठी, इलेक्ट्रॉनिक ... पद्धत वापरली जाते.
7. आकृतीनुसार, अॅल्युमिनियमने ... एक इलेक्ट्रॉन दिला.
8. प्रतिक्रियेत:
H2 + Cl2 = 2HCl
हायड्रोजन H2 - ...
9. कोणत्या प्रकारच्या प्रतिक्रिया नेहमी फक्त रेडॉक्स प्रतिक्रिया असतात?
10. साध्या पदार्थांची ऑक्सिडेशन अवस्था आहे ....
11. प्रतिक्रियेत:
कमी करणारा...
गृहपाठ असाइनमेंट.
ओ.एस. गॅब्रिलियनच्या पाठ्यपुस्तकानुसार "केमिस्ट्री -8" § 43, पी. १७८–१७९, उदा. 1, 7 लेखी. एक कार्य (घरी). पहिल्या अंतराळ यान आणि पाणबुडीच्या डिझाइनरना एका समस्येचा सामना करावा लागला: जहाज आणि स्पेस स्टेशनवर सतत हवा रचना कशी राखायची? जादा कार्बन डाय ऑक्साईडपासून मुक्त व्हा आणि ऑक्सिजन पुन्हा भरा? यावर उपाय सापडला आहे.
पोटॅशियम सुपरऑक्साइड KO2 कार्बन डायऑक्साइडशी परस्परसंवादाच्या परिणामी ऑक्सिजन बनवते:
जसे आपण पाहू शकता, ही एक रेडॉक्स प्रतिक्रिया आहे. या अभिक्रियामध्ये ऑक्सिजन हा ऑक्सिडायझिंग एजंट आणि कमी करणारा एजंट दोन्ही आहे.
अंतराळ मोहिमेत, प्रत्येक ग्रॅम मालाची गणना होते. पोटॅशियम सुपरऑक्साइडच्या पुरवठ्याची गणना करा जे स्पेस फ्लाइटमध्ये 10 दिवसांसाठी डिझाइन केले असल्यास आणि क्रूमध्ये दोन लोक असल्यास. हे ज्ञात आहे की एक व्यक्ती दररोज 1 किलो कार्बन डायऑक्साइड बाहेर टाकते.
(उत्तर. ६४.५ किलो KO2. )
कार्य ( भारदस्त पातळीअडचणी). कोलोसस ऑफ रोड्सचा नाश होऊ शकणाऱ्या रेडॉक्स प्रतिक्रियांची समीकरणे लिहा. लक्षात ठेवा की हा विशाल पुतळा आधुनिक तुर्कीच्या किनारपट्टीवरील एजियन बेटावरील एका बंदर शहरात उभा आहे, जेथे आर्द्र भूमध्यसागरीय हवा क्षारांनी भरलेली आहे. ते कांस्य (तांबे आणि कथील यांचे मिश्र धातु) बनलेले होते आणि लोखंडी चौकटीवर बसवले होते.
साहित्य
गॅब्रिलियन ओ.एस.. रसायनशास्त्र-8. मॉस्को: बस्टर्ड, 2002;
गॅब्रिलियन ओ.एस., वोस्कोबोयनिकोवा एन.पी., याशुकोवा ए.व्ही.शिक्षकाचे हँडबुक. 8वी इयत्ता. मॉस्को: बस्टर्ड, 2002;
कॉक्स आर., मॉरिस एन. जगातील सात आश्चर्ये. प्राचीन जग, मध्य युग, आमचा काळ. M.: BMM AO, 1997;
लहान मुलांचा ज्ञानकोश. रसायनशास्त्र. एम.: रशियन विश्वकोशीय भागीदारी, 2001; मुलांसाठी विश्वकोश "अवंत +". रसायनशास्त्र. टी. 17. एम.: अवंता+, 2001;
खोमचेन्को G.P., Sevastyanova K.I.रेडॉक्स प्रतिक्रिया. मॉस्को: शिक्षण, 1989.
एसपी लेबेशेवा,
हायस्कूल रसायनशास्त्र शिक्षक क्र. 8
(बाल्टिस्क, कॅलिनिनग्राड प्रदेश)
गुणांक निवडण्याचे नियम:
- जर प्रतिक्रिया योजनेच्या एका भागातील घटकाच्या अणूंची संख्या सम आणि दुसऱ्या भागात विषम असेल, तर गुणांक 2 हे सूत्रासमोर विषम संख्येच्या अणूंसह ठेवले पाहिजे आणि नंतर सर्वांची संख्या अणू समान करणे आवश्यक आहे.
- गुणांकांची नियुक्ती रचनातील सर्वात जटिल पदार्थापासून सुरू झाली पाहिजे आणि हे खालील क्रमाने करा:
प्रथम तुम्हाला धातूच्या अणूंची संख्या, नंतर अम्लीय अवशेष (नॉन-मेटल अणू), नंतर हायड्रोजन अणू आणि शेवटी, ऑक्सिजन अणूंची संख्या समान करणे आवश्यक आहे.
- समीकरणाच्या डाव्या आणि उजव्या भागांमध्ये ऑक्सिजन अणूंची संख्या समान असल्यास, गुणांक योग्यरित्या निर्धारित केले जातात.
- त्यानंतर, समीकरणाच्या भागांमधील बाण समान चिन्हाने बदलला जाऊ शकतो.
- रासायनिक अभिक्रिया समीकरणातील गुणांकांमध्ये समान विभाजक नसावेत.
उदाहरण. लोह (III) हायड्रॉक्साईड आणि सल्फ्यूरिक ऍसिड यांच्यात लोह (III) सल्फेटच्या निर्मितीसह रासायनिक अभिक्रियाचे समीकरण बनवू.
1. एक प्रतिक्रिया योजना बनवूया:
Fe(OH)3 + H2SO4 → Fe2(SO4)3 + H2O
2. आम्ही पदार्थांच्या सूत्रांसाठी गुणांक निवडतो. आपल्याला माहित आहे की आपण सर्वात जटिल पदार्थापासून सुरुवात केली पाहिजे आणि संपूर्ण योजनेत प्रथम धातूचे अणू, नंतर ऍसिडचे अवशेष, नंतर हायड्रोजन आणि शेवटी ऑक्सिजनचे समानीकरण केले पाहिजे. आमच्या योजनेत, सर्वात जटिल पदार्थ Fe2(SO4)3 आहे. त्यात दोन लोह अणू असतात आणि Fe(OH)3 मध्ये एक लोह अणू असतो. तर, सूत्र Fe (OH) 3 च्या आधी गुणांक 2 ठेवणे आवश्यक आहे:
2Fe(OH)3 + H2SO4 → Fe2(SO4)3 + H2O
आता आपण SO4 ऍसिड अवशेषांची संख्या समान करतो. Fe2(SO4)3 मीठामध्ये तीन SO4 ऍसिडचे अवशेष असतात. तर, डाव्या बाजूला, H2SO4 सूत्रापूर्वी, आम्ही गुणांक 3 ठेवतो:
2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + H2O.
आता आपण हायड्रोजन अणूंची संख्या समान करतो. आकृतीच्या डाव्या बाजूला लोह हायड्रॉक्साईड 2Fe (OH) 3 - 6 हायड्रोजन अणू (2
3), सल्फ्यूरिक ऍसिड 3H2SO4 मध्ये - 6 हायड्रोजन अणू देखील.
रासायनिक समीकरणांमध्ये गुणांक कसे लावायचे
एकूण, डाव्या बाजूला 12 हायड्रोजन अणू आहेत. तर, उजव्या बाजूला, आम्ही H2O पाण्याच्या सूत्रासमोर 6 चा एक घटक ठेवतो - आणि आता उजव्या बाजूला 12 हायड्रोजन अणू देखील आहेत:
2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6H2O.
ऑक्सिजन अणूंची संख्या समान करणे बाकी आहे. परंतु हे यापुढे आवश्यक नाही, कारण आकृतीच्या डाव्या आणि उजव्या भागांमध्ये आधीच ऑक्सिजन अणूंची संख्या समान आहे - प्रत्येक भागामध्ये 18. याचा अर्थ असा की सर्किट पूर्ण लिहिलेले आहे आणि आम्ही बाण समान चिन्हाने बदलू शकतो:
2Fe(OH)3 + 3H2SO4 = Fe2(SO4)3 + 6H2O.
शिक्षण
रासायनिक समीकरणांमध्ये गुणांक कसे लावायचे? रासायनिक समीकरणे
आज आपण रासायनिक समीकरणांमध्ये गुणांकांची मांडणी कशी करावी याबद्दल बोलू. हा प्रश्न केवळ शैक्षणिक संस्थांच्या उच्च माध्यमिक विद्यार्थ्यांसाठीच नाही तर अशा मुलांसाठी देखील स्वारस्य आहे ज्यांना कॉम्प्लेक्सच्या मूलभूत घटकांशी परिचित होत आहे आणि मनोरंजक विज्ञान. जर पहिल्या टप्प्यावर तुम्हाला रासायनिक समीकरणे कशी लिहायची हे समजले असेल, तर भविष्यात समस्या सोडवण्यात कोणतीही अडचण येणार नाही. चला सुरुवातीपासूनच ते मिळवूया.
काय समीकरण आहे
त्याद्वारे निवडलेल्या अभिकर्मकांमध्ये होणाऱ्या रासायनिक अभिक्रियाची सशर्त रेकॉर्ड असा अर्थ लावण्याची प्रथा आहे. अशा प्रक्रियेसाठी, निर्देशांक, गुणांक, सूत्रे वापरली जातात.
संकलन अल्गोरिदम
रासायनिक समीकरणे कशी लिहायची? मूळ संयुगे एकत्रित करून कोणत्याही परस्परसंवादाची उदाहरणे लिहिली जाऊ शकतात. समान चिन्ह हे सूचित करते की प्रतिक्रिया देणाऱ्या पदार्थांमध्ये परस्परसंवाद आहे. पुढे, व्हॅलेन्सी (ऑक्सिडेशन स्थिती) द्वारे उत्पादनांसाठी एक सूत्र संकलित केले आहे.
संबंधित व्हिडिओ
प्रतिक्रिया कशी नोंदवायची
उदाहरणार्थ, तुम्हाला मिथेनच्या गुणधर्मांची पुष्टी करणारी रासायनिक समीकरणे लिहायची असल्यास, खालील पर्याय निवडा:
- हॅलोजनेशन (डी. आय. मेंडेलीव्हच्या नियतकालिक सारणीच्या VIIA घटकासह मूलगामी परस्परसंवाद);
- वातावरणातील ऑक्सिजनमध्ये ज्वलन.

पहिल्या प्रकरणात, आम्ही डाव्या बाजूला प्रारंभिक पदार्थ आणि उजवीकडे परिणामी उत्पादने लिहितो. प्रत्येक रासायनिक घटकाच्या अणूंची संख्या तपासल्यानंतर, आम्ही चालू प्रक्रियेची अंतिम नोंद मिळवतो. जेव्हा वातावरणातील ऑक्सिजनमध्ये मिथेन जळते तेव्हा एक एक्झोथर्मिक प्रक्रिया उद्भवते, परिणामी कार्बन डायऑक्साइड आणि पाण्याची वाफ तयार होते.
रासायनिक समीकरणांमध्ये गुणांक योग्यरित्या ठेवण्यासाठी, पदार्थांच्या वस्तुमानाच्या संवर्धनाचा नियम वापरला जातो. आम्ही कार्बन अणूंची संख्या निर्धारित करून समायोजन प्रक्रिया सुरू करतो. पुढे, आम्ही हायड्रोजनची गणना करतो आणि त्यानंतरच आम्ही ऑक्सिजनचे प्रमाण तपासतो.
OVR
इलेक्ट्रॉनिक समतोल किंवा अर्ध-प्रतिक्रियांच्या पद्धतीचा वापर करून जटिल रासायनिक समीकरणे समान केली जाऊ शकतात. आम्ही खालील प्रकारच्या प्रतिक्रियांमध्ये गुणांक व्यवस्थित करण्यासाठी डिझाइन केलेल्या क्रियांचा क्रम ऑफर करतो:

प्रथम, कंपाऊंडमधील प्रत्येक घटकाची ऑक्सिडेशन स्थिती व्यवस्थित करणे महत्वाचे आहे. त्यांना ठेवताना, काही नियम विचारात घेणे आवश्यक आहे:
- साध्या पदार्थासाठी ते शून्य असते.
- बायनरी कंपाऊंडमध्ये त्यांची बेरीज 0 असते.
- तीन किंवा अधिक घटकांच्या संयुगात, पहिल्याचे सकारात्मक मूल्य असते आणि शेवटच्या आयनमध्ये ऑक्सिडेशन स्थितीचे नकारात्मक मूल्य असते. मध्यवर्ती घटकाची बेरीज 0 असावी हे लक्षात घेऊन गणिती पद्धतीने मोजले जाते.
पुढे, ते अणू किंवा आयन निवडले जातात ज्यासाठी ऑक्सिडेशन स्थिती बदलली आहे. अधिक आणि वजा चिन्हे इलेक्ट्रॉनची संख्या दर्शवतात (स्वीकारलेले, दिलेले). पुढे, त्यांच्यामध्ये सर्वात लहान गुणाकार निर्धारित केला जातो. एनओसीला या आकड्यांद्वारे विभाजित केल्यावर क्रमांक मिळतात. हे अल्गोरिदम रासायनिक समीकरणांमध्ये गुणांक कसे व्यवस्थित करायचे या प्रश्नाचे उत्तर असेल.
पहिले उदाहरण
समजा कार्य दिले आहे: "प्रतिक्रियेतील गुणांक व्यवस्थित करा, अंतर भरा, ऑक्सिडायझिंग एजंट आणि कमी करणारे एजंट निश्चित करा." अशी उदाहरणे शालेय पदवीधरांना दिली जातात ज्यांनी त्यांची परीक्षा म्हणून रसायनशास्त्र निवडले आहे.
KMnO4 + H2SO4 + KBr = MnSO4 + Br2 +…+…

भविष्यातील अभियंते आणि चिकित्सकांना ऑफर केलेल्या रासायनिक समीकरणांमधील गुणांक कसे व्यवस्थित करावे हे समजून घेण्याचा प्रयत्न करूया. प्रारंभिक सामग्री आणि उपलब्ध उत्पादनांमधील घटकांच्या ऑक्सिडेशन स्थितीची मांडणी केल्यानंतर, आम्हाला आढळले की मॅंगनीज आयन ऑक्सिडायझिंग एजंट म्हणून कार्य करते आणि ब्रोमाइड आयन कमी करण्याचे गुणधर्म दर्शविते.
आम्ही असा निष्कर्ष काढतो की गहाळ पदार्थ रेडॉक्स प्रक्रियेत भाग घेत नाहीत. गहाळ उत्पादनांपैकी एक पाणी आहे, आणि दुसरे पोटॅशियम सल्फेट असेल. इलेक्ट्रॉनिक शिल्लक संकलित केल्यानंतर, समीकरणातील गुणांकांची सेटिंग ही अंतिम पायरी असेल.
दुसरे उदाहरण
रेडॉक्स प्रकाराच्या रासायनिक समीकरणांमध्ये गुणांक कसे व्यवस्थित करायचे हे समजून घेण्यासाठी दुसरे उदाहरण देऊ.
समजा आमच्याकडे खालील स्कीमा आहे:
P + HNO3 = NO2 +…+…
फॉस्फरस, जो नियमानुसार एक साधा पदार्थ आहे, कमी करणारे गुणधर्म प्रदर्शित करतो, ऑक्सिडेशन स्थिती +5 पर्यंत वाढवतो. म्हणून, गहाळ पदार्थांपैकी एक फॉस्फोरिक ऍसिड H3PO4 असेल. OVR कमी करणाऱ्या एजंटची उपस्थिती गृहीत धरते, जे नायट्रोजन असेल. ते नायट्रिक ऑक्साईड (4) मध्ये जाते, NO2 बनवते

या अभिक्रियामध्ये गुणांक ठेवण्यासाठी, आम्ही इलेक्ट्रॉनिक शिल्लक बनवू.
P0 5e = P+5 देते
N+5 घेते e = N+4
नायट्रिक ऍसिड आणि नायट्रिक ऑक्साईड (4) 5 च्या घटकापूर्वी असणे आवश्यक आहे हे लक्षात घेता, आम्हाला पूर्ण प्रतिक्रिया मिळते:
P + 5HNO3 = 5NO2 + H2O + H3PO4
रसायनशास्त्रातील स्टिरिओकेमिकल गुणांक विविध संगणकीय समस्या सोडविण्यास अनुमती देतात.
तिसरे उदाहरण
गुणांकांची नियुक्ती अनेक हायस्कूल विद्यार्थ्यांना अडचणी निर्माण करते हे लक्षात घेता, विशिष्ट उदाहरणे वापरून क्रियांचा क्रम तयार करणे आवश्यक आहे. आम्ही कार्याचे आणखी एक उदाहरण देतो, ज्याच्या अंमलबजावणीसाठी रेडॉक्स प्रतिक्रियेतील गुणांक व्यवस्थित करण्याच्या पद्धतीवर प्रभुत्व असणे आवश्यक आहे.
H2S + HMnO4 = S + MnO2 +…

प्रस्तावित कार्याची वैशिष्ठ्य अशी आहे की गहाळ प्रतिक्रिया उत्पादनास पूरक करणे आवश्यक आहे आणि त्यानंतरच आपण गुणांक सेट करण्यास पुढे जाऊ शकता.
यौगिकांमधील प्रत्येक घटकाच्या ऑक्सिडेशन स्थितीची मांडणी केल्यानंतर, असा निष्कर्ष काढला जाऊ शकतो की मॅंगनीज, जे व्हॅलेन्स कमी करते, ऑक्सिडायझिंग गुणधर्म प्रदर्शित करते. सल्फर प्रस्तावित प्रतिक्रियेमध्ये कमी करण्याची क्षमता दाखवते, एका साध्या पदार्थात कमी केले जाते. इलेक्ट्रॉनिक शिल्लक संकलित केल्यानंतर, आम्हाला केवळ प्रस्तावित प्रक्रिया योजनेमध्ये गुणांक ठेवावे लागतील. आणि कृत्य झाले आहे.
चौथे उदाहरण
रासायनिक समीकरणजेव्हा पदार्थांच्या वस्तुमानाच्या संरक्षणाचा नियम त्यात पूर्णपणे पाळला जातो तेव्हा त्याला पूर्ण प्रक्रिया म्हणतात. हा नमुना कसा तपासायचा? अभिक्रियामध्ये प्रवेश केलेल्या समान प्रकारच्या अणूंची संख्या परस्परसंवाद उत्पादनांमधील त्यांच्या संख्येशी संबंधित असणे आवश्यक आहे. केवळ या प्रकरणात रेकॉर्ड केलेल्या रासायनिक परस्परसंवादाची उपयुक्तता, गणनेसाठी त्याचा वापर करण्याची शक्यता, संगणकीय समस्या सोडवणे याबद्दल बोलणे शक्य होईल. विविध स्तरअडचणी येथे कार्याचा एक प्रकार आहे, ज्यामध्ये प्रतिक्रियेतील गहाळ स्टिरिओकेमिकल गुणांकांची व्यवस्था समाविष्ट आहे:
Si + …+ HF = H2SiF6 + नाही +…

कार्याची जटिलता अशी आहे की प्रारंभिक पदार्थ आणि परस्परसंवादाची उत्पादने दोन्ही वगळण्यात आली आहेत. ऑक्सिडेशन स्थितीचे सर्व घटक सेट केल्यानंतर, आम्ही पाहतो की सिलिकॉन अणू प्रस्तावित कार्यामध्ये कमी गुणधर्म प्रदर्शित करतो. नायट्रोजन (II) प्रतिक्रिया उत्पादनांमध्ये उपस्थित आहे, सुरुवातीच्या संयुगांपैकी एक नायट्रिक ऍसिड आहे. तार्किकदृष्ट्या, आम्ही निर्धारित करतो की प्रतिक्रियेचे गहाळ उत्पादन पाणी आहे. अंतिम टप्पा प्रतिक्रिया मध्ये प्राप्त स्टिरिओकेमिकल गुणांकांची व्यवस्था असेल.
3Si + 4HNO3 + 18HF = 3H2SiF6 + 4NO + 8H2O
समीकरण समस्येचे उदाहरण
हायड्रोजन क्लोराईडच्या 10% द्रावणाचे प्रमाण निश्चित करणे आवश्यक आहे, ज्याची घनता 1.05 ग्रॅम / एमएल आहे, त्याच्या कार्बाइडच्या हायड्रोलिसिस दरम्यान तयार झालेल्या कॅल्शियम हायड्रॉक्साईडच्या संपूर्ण तटस्थतेसाठी आवश्यक आहे. हे ज्ञात आहे की हायड्रोलिसिस दरम्यान सोडलेला वायू 8.96 लिटर (n.a.) ची मात्रा व्यापतो.
CaC2 + 2H2O = Ca(OH)2 + C2H2
कॅल्शियम हायड्रॉक्साईड हायड्रोजन क्लोराईडशी संवाद साधते, पूर्ण तटस्थीकरण होते:
Ca(OH)2 + 2HCl = CaCl2 + 2H2O

आम्ही या प्रक्रियेसाठी आवश्यक असलेल्या आम्लाच्या वस्तुमानाची गणना करतो.
रासायनिक समीकरणांमधील गुणांक आणि निर्देशांक
हायड्रोजन क्लोराईड द्रावणाची मात्रा निश्चित करा. समस्येची सर्व गणना स्टिरिओकेमिकल गुणांक लक्षात घेऊन केली जाते, जे त्यांचे महत्त्व पुष्टी करते.
शेवटी
रसायनशास्त्रातील युनिफाइड स्टेट परीक्षेच्या निकालांचे विश्लेषण असे सूचित करते की समीकरणांमध्ये स्टिरिओकेमिकल गुणांक सेट करणे, इलेक्ट्रॉनिक शिल्लक संकलित करणे, ऑक्सिडायझिंग एजंट निश्चित करणे आणि कमी करणारे एजंट आधुनिक पदवीधरांसाठी गंभीर अडचणी निर्माण करतात. सामान्य शिक्षण शाळा. दुर्दैवाने, आधुनिक पदवीधरांच्या स्वातंत्र्याची डिग्री व्यावहारिकदृष्ट्या कमी आहे, म्हणून हायस्कूलचे विद्यार्थी शिक्षकाने प्रस्तावित केलेल्या सैद्धांतिक आधारावर काम करत नाहीत.
मध्ये सामान्य चुका, ज्याला शाळकरी मुले प्रतिक्रियांमध्ये गुणांक ठेवून परवानगी देतात भिन्न प्रकार, अनेक गणिती चुका. उदाहरणार्थ, किमान सामान्य गुणक कसे शोधायचे, भागाकार आणि गुणाकार योग्यरित्या कसा करायचा हे प्रत्येकाला माहित नाही. या घटनेचे कारण म्हणजे या विषयाच्या अभ्यासासाठी शैक्षणिक शाळांमध्ये वाटप केलेल्या तासांची संख्या कमी होणे. रसायनशास्त्रातील मूलभूत कार्यक्रमासह, शिक्षकांना त्यांच्या विद्यार्थ्यांच्या रेडॉक्स प्रक्रियेतील इलेक्ट्रॉनिक शिल्लक संकलनाशी संबंधित समस्यांसह कार्य करण्याची संधी नसते.
शिक्षण
चौरस म्हणजे काय? चौकोनाचे शिरोबिंदू, विभाग, समतल, समीकरण, खंड, पायाचे क्षेत्रफळ आणि कोन कसे शोधायचे?
चौकोन म्हणजे काय या प्रश्नाची अनेक उत्तरे असू शकतात. तुम्ही हा प्रश्न कोणाला विचारता यावर हे सर्व अवलंबून आहे. संगीतकार म्हणेल की स्क्वेअर 4, 8, 16, 32 बार किंवा जाझ इम्प्रोव्हायझेशन आहे. मुल - हे काय...
गाड्या
कारमध्ये अँटीफ्रीझ किती वेळा बदलावे?
कार इंजिनच्या ऑपरेशन दरम्यान, त्याच्या सिलेंडर्समधील वायूंचे तापमान 2000 अंशांपर्यंत पोहोचते. यामुळे, पॉवर युनिटच्या भागांचे मजबूत गरम होते. इंजिनमधून अतिरिक्त उष्णता काढून टाकण्यासाठी, ...
गाड्या
कार थर्मोस्टॅट कसे कार्य करते? ऑपरेटिंग तत्त्व
कोणतीही आधुनिक कार कूलिंग सिस्टमशिवाय पूर्ण होत नाही. ज्वलनशील मिश्रणाच्या प्रक्रियेदरम्यान इंजिनमधून निघणारी सर्व उष्णता तीच घेते. पिस्टन हलत आहेत, मिश्रण जळत आहे, अनुक्रमे, आपल्याला चांगली गरज आहे ...
गाड्या
आपल्या स्वत: च्या हातांनी कारमध्ये एअर कंडिशनर कसे भरायचे? मी माझ्या कारमध्ये किती वेळा एअर कंडिशनर भरावे? मी कारमधील एअर कंडिशनर कुठे चार्ज करू शकतो?
कार एअर कंडिशनिंग आज केवळ एक लक्झरी नाही तर एक आवश्यक वाहन साधन आहे जे केबिनमधील अनुकूल मायक्रोक्लीमेटसाठी जबाबदार आहे. जवळजवळ सर्व आधुनिक कार मॉडेल्स सुसज्ज आहेत, हवामान नसल्यास…
गाड्या
आपल्या स्वत: च्या हातांनी कारमधील एअर कंडिशनर कसे स्वच्छ करावे?
कार मालकांनी त्यांच्या वाहनाच्या मुख्य भाग आणि यंत्रणेच्या स्थितीची सतत काळजी घेतली पाहिजे. तथापि, त्यांना स्वच्छ आणि चांगल्या स्थितीत ठेवणे आपल्याला सुरक्षिततेची इष्टतम पातळी प्राप्त करण्यास अनुमती देते ...
गाड्या
गियर तेल 80W90: वैशिष्ट्ये, निवड, पुनरावलोकने. मॅन्युअल गिअरबॉक्समध्ये कोणत्या प्रकारचे तेल भरायचे?
गियर ऑइल 80W90, ज्याची वैशिष्ट्ये आज आपण विचारात घेणार आहोत, 85W90 आणि 75W90 च्या व्हिस्कोसिटी वर्गांमधील सरासरीला श्रेय दिले जाऊ शकते. ते एकमेकांपेक्षा कोणते गुणात्मक वैशिष्ट्ये वेगळे आहेत ते अधिक तपशीलवार शोधूया ...
गाड्या
पॉवर स्टीयरिंगमध्ये कोणत्या प्रकारचे तेल भरायचे? पॉवर स्टीयरिंग ऑइल बदलण्याच्या टिपा
पॉवर स्टीयरिंगला, कारचे इतर घटक आणि असेंब्ली प्रमाणेच, वेळोवेळी देखभाल आवश्यक असते. बहुतेकदा, सर्व प्रतिबंधात्मक उपाय कार्यरत द्रवपदार्थ बदलण्यासाठी खाली येतात. अनेकदा तुम्हाला फक्त गरज असते...
गाड्या
मॉस्कोमध्ये पार्किंगसाठी पैसे कसे द्यावे? नियम सशुल्क पार्किंग
सशुल्क पार्किंगसाठी नियम आहेत, जे मॉस्को वाहन चालकाचे जीवन सुलभ करण्यासाठी तयार केले आहेत. पार्किंग हे रहस्य नाही वाहनराजधानीत हे सोपे नाही: शहरातील रस्त्यांच्या कडेला गर्दीने भरलेली आहे…
गाड्या
आपल्या स्वत: च्या हातांनी कारमध्ये सुगंध कसे बनवायचे
प्रत्येक कार मालकाला त्याच्या केबिनमध्ये हवे असते लोखंडी घोडानेहमी एक आनंददायी आणि आवडते चव सादर करा. कुणाला कॉफीचा वास आवडतो, कुणाला लिंबूवर्गीय फळे आवडतात आणि कुणाला ताजेपणा आवडतो. काय चव...
गाड्या
घरी बॅटरी कशी चार्ज करावी?
कदाचित प्रत्येक कार मालकाने मृत बॅटरीच्या समस्येचा सामना केला असेल. जर तुम्ही कारच्या उर्जा स्त्रोताकडे पुरेसे लक्ष दिले नाही तर हा त्रास कोणत्याही ड्रायव्हरला होऊ शकतो. आम्ही याबद्दल बोलू…
पर्याय 1
a) Na + O2 -> Na2O d) H2 + F2 -> HF
b) CaCO3-> CaO + CO2 e) H2O + K2O -> KOH
c) Zn + H2SO4 -> H2 + ZnSO4 f) Cu(OH)2 + HNO3 -> Cu(NO3)2 + H2O
धडा 13
व्याख्या लिहा:
a) कंपाऊंड प्रतिक्रिया ब) एक्झोथर्मिक प्रतिक्रिया c) अपरिवर्तनीय प्रतिक्रिया.
a) कार्बन ऑक्सिजनशी संवाद साधतो आणि कार्बन मोनोऑक्साइड (II) तयार होतो;
b) मॅग्नेशियम ऑक्साईड नायट्रिक ऍसिड आणि मॅग्नेशियम नायट्रेट आणि पाणी तयार होते.
क) लोह (III) हायड्रॉक्साईड लोह ऑक्साईड (III) आणि पाण्यात विघटित होते;
d) ऑक्सिजन आणि कार्बन मोनोऑक्साइड (IV) मध्ये मिथेन CH4 जळते आणि पाणी तयार होते;
e) नायट्रिक ऑक्साईड (V) पाण्यात विरघळल्यावर नायट्रिक आम्ल बनते.
4. समीकरणानुसार समस्या सोडवा:
अ) हायड्रोजन फ्लोरिनवर प्रतिक्रिया देतो तेव्हा हायड्रोजन फ्लोराईडची किती मात्रा तयार होते?
b) 80% CaCO3 असलेल्या चुनखडीच्या विघटनादरम्यान कॅल्शियम ऑक्साईडचे किती वस्तुमान तयार होते?
c) 35% अशुद्धता असलेल्या जस्त सल्फ्यूरिक ऍसिडशी संवाद साधताना हायड्रोजनचे किती प्रमाण आणि वस्तुमान सोडले जाईल?
पर्याय २
- गुणांकांची मांडणी करा, रासायनिक अभिक्रियाचा प्रकार निश्चित करा, सूत्रांखाली पदार्थांची नावे लिहा:
a) P + O2 -> P2O5 d) H2 + N2 -> NH3
b) CaCO3 + HCl -> CaCl2 + H2O + CO2 e) H2O + Li2O -> LiOH
c) Mg + H2SO4 -> H2 + MgSO4 e) Ca(OH)2 + HNO3 -> Ca(NO3)2 + H2O
2. व्याख्या लिहा:
a) विघटन प्रतिक्रिया b) एंडोथर्मिक प्रतिक्रिया c) उत्प्रेरक प्रतिक्रिया.
3. वर्णनानुसार समीकरणे लिहा:
अ) कार्बन ऑक्सिजनशी संवाद साधतो आणि कार्बन मोनोऑक्साइड (IV) तयार होतो;
b) बेरियम ऑक्साईड नायट्रिक ऍसिड आणि बेरियम नायट्रेट आणि पाणी तयार होते;
c) अॅल्युमिनियम हायड्रॉक्साईड अॅल्युमिनियम ऑक्साईड आणि पाण्यात विघटित होते;
ड) अमोनिया NH3 ऑक्सिजन आणि नायट्रोजन आणि पाण्यात जळते आणि पाणी तयार होते;
e) फॉस्फरस (V) ऑक्साईड, पाण्यात विरघळल्यावर फॉस्फरिक ऍसिड बनते.
4. समीकरणानुसार समस्या सोडवा:
अ) हायड्रोजनची नायट्रोजनशी अभिक्रिया झाल्यावर अमोनियाची किती मात्रा तयार होते?
b) 80% CaCO3 असलेल्या मार्बलच्या हायड्रोक्लोरिक ऍसिडशी परस्परसंवाद केल्यावर कॅल्शियम क्लोराईडचे किती वस्तुमान तयार होते?
c) 30% अशुद्धता असलेल्या मॅग्नेशियम सल्फ्यूरिक ऍसिडशी संवाद साधताना हायड्रोजनचे किती प्रमाण आणि वस्तुमान सोडले जाईल?
 रासायनिक समीकरणे कशी लिहायची? प्रथम, कंपाऊंडमधील प्रत्येक घटकाची ऑक्सिडेशन स्थिती व्यवस्थित करणे महत्वाचे आहे. समजा कार्य दिले आहे: "प्रतिक्रियेतील गुणांक व्यवस्थित करा, अंतर भरा, ऑक्सिडायझिंग एजंट आणि कमी करणारे एजंट निश्चित करा." गहाळ उत्पादनांपैकी एक पाणी आहे, आणि दुसरे पोटॅशियम सल्फेट असेल. इलेक्ट्रॉनिक शिल्लक संकलित केल्यानंतर, समीकरणातील गुणांकांची सेटिंग ही अंतिम पायरी असेल. समस्येची सर्व गणना स्टिरिओकेमिकल गुणांक लक्षात घेऊन केली जाते, जे त्यांचे महत्त्व पुष्टी करते. विविध प्रकारच्या प्रतिक्रियांमध्ये गुणांक टाकताना शाळकरी मुले ज्या ठराविक चुका करतात, त्यात अनेक गणिती चुका आहेत.
रासायनिक समीकरणे कशी लिहायची? प्रथम, कंपाऊंडमधील प्रत्येक घटकाची ऑक्सिडेशन स्थिती व्यवस्थित करणे महत्वाचे आहे. समजा कार्य दिले आहे: "प्रतिक्रियेतील गुणांक व्यवस्थित करा, अंतर भरा, ऑक्सिडायझिंग एजंट आणि कमी करणारे एजंट निश्चित करा." गहाळ उत्पादनांपैकी एक पाणी आहे, आणि दुसरे पोटॅशियम सल्फेट असेल. इलेक्ट्रॉनिक शिल्लक संकलित केल्यानंतर, समीकरणातील गुणांकांची सेटिंग ही अंतिम पायरी असेल. समस्येची सर्व गणना स्टिरिओकेमिकल गुणांक लक्षात घेऊन केली जाते, जे त्यांचे महत्त्व पुष्टी करते. विविध प्रकारच्या प्रतिक्रियांमध्ये गुणांक टाकताना शाळकरी मुले ज्या ठराविक चुका करतात, त्यात अनेक गणिती चुका आहेत.
काही नियम आहेत ज्याद्वारे ते प्रत्येक घटकासाठी निर्धारित केले जाऊ शकतात. ऑक्सिडेशन अवस्था मोजण्यासाठी तीन घटकांचा समावेश असलेल्या सूत्रांचे स्वतःचे बारकावे आहेत. इलेक्ट्रॉन बॅलन्स पद्धतीचा वापर करून रासायनिक समीकरणे कशी समान करायची याबद्दल संभाषण सुरू ठेवूया. डाव्या आणि उजव्या भागांमधील प्रत्येक घटकाची संख्या तपासणे ही एक पूर्व शर्त आहे. गुणांक योग्यरित्या ठेवले असल्यास, त्यांची संख्या समान असावी.
बीजगणित पद्धत
प्रायोगिक सूत्रे आणि रासायनिक विश्लेषणाच्या तपशीलवार पाहण्यासाठी मूलभूत विश्लेषणाबद्दल वाचा.
रसायनशास्त्र पदार्थ, त्यांचे गुणधर्म आणि परिवर्तनांचा अभ्यास करते. आण्विक स्वरूपात, वातावरणातील लोहाच्या ज्वलनाची प्रक्रिया चिन्हे आणि चिन्हे वापरून व्यक्त केली जाऊ शकते. पदार्थांच्या वस्तुमानाच्या संवर्धनाच्या कायद्यानुसार, उत्पादनाच्या सूत्रासमोर 2 चा घटक ठेवणे आवश्यक आहे. पुढे, कॅल्शियम तपासले जाते. सुरुवातीला, प्रारंभिक पदार्थ आणि परस्परसंवाद उत्पादनांमधील प्रत्येक घटकासाठी, आम्ही ऑक्सिडेशन स्थितींची मूल्ये ठेवू. पुढील पायरी म्हणजे हायड्रोजनची चाचणी करणे.
रासायनिक अभिक्रियांचे समीकरण
साध्या रासायनिक समीकरणातून पूर्ण प्राप्त करण्यासाठी रासायनिक अभिक्रियांचे समीकरण आवश्यक आहे. चला कार्बनपासून सुरुवात करूया.
वस्तुमानाच्या संवर्धनाचा नियम नवीन अणूंचा देखावा आणि रासायनिक अभिक्रिया दरम्यान जुन्या अणूंचा नाश वगळतो. प्रत्येक अणूच्या निर्देशांकाकडे लक्ष द्या, तोच त्यांची संख्या दर्शवितो. समीकरणाच्या उजव्या बाजूला असलेल्या पदार्थांच्या रेणूंसमोर निर्देशांक जोडून, आम्ही ऑक्सिजन अणूंची संख्या देखील बदलली. आता सर्व कार्बन, हायड्रोजन आणि ऑक्सिजन अणूंची संख्या समीकरणाच्या दोन्ही बाजूंना समान आहे.
ते म्हणतात की जर घटक कंसाच्या बाहेर असेल, तर कंसातील प्रत्येक घटक त्याच्याशी गुणाकार केला जातो. आपल्याला नायट्रोजनपासून प्रारंभ करणे आवश्यक आहे, कारण ते ऑक्सिजन आणि हायड्रोजनपेक्षा कमी आहे. ग्रेट, हायड्रोजन समान. पुढे बेरियम आहे. ते समतल केले आहे, त्याला स्पर्श करणे आवश्यक नाही. प्रतिक्रिया करण्यापूर्वी, दोन क्लोरीन आहेत, त्यानंतर - फक्त एक. काय करावे लागेल? आता, नुकत्याच सेट केलेल्या गुणांकामुळे, प्रतिक्रियेनंतर, दोन सोडियम प्राप्त झाले, आणि प्रतिक्रियेपूर्वी देखील दोन. छान, बाकी सर्व काही संतुलित आहे. ऑक्सिडेशन कुठे झाले आणि कुठे घट झाली हे समजून घेण्यासाठी प्रत्येक पदार्थातील सर्व घटकांच्या ऑक्सिडेशन अवस्थांची मांडणी करणे ही पुढील पायरी आहे.

साध्या प्रतिक्रियांचे विश्लेषण करण्याचे उदाहरण
उजव्या बाजूला कोणतेही निर्देशांक नाहीत, म्हणजे, ऑक्सिजनचा एक कण आणि डावीकडे - 2 कण. रासायनिक सूत्रामध्ये कोणतेही अतिरिक्त निर्देशांक किंवा दुरुस्त्या केल्या जाऊ शकत नाहीत, कारण ते योग्यरित्या लिहिलेले आहे. उजव्या बाजूला, 2 ऑक्सिजन आयन मिळविण्यासाठी आपण एकाला 2 ने गुणाकार करतो.
कार्यास पुढे जाण्यापूर्वी, आपल्याला हे शिकण्याची आवश्यकता आहे की रासायनिक घटक किंवा संपूर्ण सूत्रासमोर ठेवलेल्या संख्येला गुणांक म्हणतात. आम्ही विश्लेषण सुरू करतो. अशा प्रकारे, समान चिन्हाच्या आधी आणि नंतर प्रत्येक घटकाच्या अणूंची संख्या समान आहे. हे लक्षात ठेवा की गुणांक निर्देशांकाने गुणाकार केला जातो आणि जोडला जात नाही.
खालील अटींच्या अधीन राहून तुम्ही तुमच्या स्वत:च्या हेतूंसाठी कोणतेही दस्तऐवज वापरण्यास मोकळे आहात:
२) रासायनिक घटकांची चिन्हे नियतकालिक सारणीमध्ये ज्या स्वरूपात दिसतात त्या स्वरूपात काटेकोरपणे लिहिल्या पाहिजेत.
माहिती कार्ड. "रासायनिक अभिक्रियांच्या समीकरणांमध्ये गुणांक ठेवण्यासाठी अल्गोरिदम."
3) कधीकधी अशी परिस्थिती उद्भवते जेव्हा अभिक्रिया आणि उत्पादनांची सूत्रे अगदी अचूकपणे लिहिली जातात, परंतु गुणांक अद्याप ठेवलेले नाहीत. अशा समस्येची सर्वात संभाव्य घटना सेंद्रिय पदार्थांच्या ऑक्सिडेशन प्रतिक्रियांसह आहे ज्यामध्ये कार्बनचा सांगाडा फाटला जातो.
प्रतिक्रिया समीकरण केवळ लिहिण्यासच नव्हे तर वाचण्यास देखील सक्षम असणे आवश्यक आहे. म्हणून, कधीकधी, प्रतिक्रिया समीकरणातील सर्व सूत्रे लिहून ठेवल्यानंतर, समीकरणाच्या प्रत्येक भागामध्ये अणूंची संख्या समान करणे आवश्यक असते - गुणांकांची व्यवस्था करणे. समीकरणाच्या डाव्या आणि उजव्या बाजूला प्रत्येक घटकाचे अणू समान आहेत की नाही ते मोजा.
बर्याच शाळकरी मुलांसाठी, रासायनिक अभिक्रियांचे समीकरण लिहिणे आणि गुणांक योग्यरित्या व्यवस्थित करणे हे सोपे काम नाही. परंतु आपल्याला फक्त काही लक्षात ठेवण्याची आवश्यकता आहे साधे नियम, आणि कार्य यापुढे अडचणी निर्माण करणार नाही. गुणांक, म्हणजे रासायनिक रेणूच्या सूत्रासमोरील संख्या, सर्व चिन्हांना लागू होते आणि प्रत्येक चिन्हाच्या प्रत्येक निर्देशांकाने गुणाकार केला जातो!
आज आपण रासायनिक समीकरणांमध्ये गुणांकांची मांडणी कशी करावी याबद्दल बोलू. हा प्रश्न केवळ शैक्षणिक संस्थांच्या उच्च माध्यमिक विद्यार्थ्यांसाठीच नाही तर जटिल आणि मनोरंजक विज्ञानाच्या मूलभूत घटकांशी परिचित असलेल्या मुलांसाठी देखील स्वारस्य आहे. पहिल्या टप्प्यावर समजून घेतल्यास, भविष्यात समस्या सोडवताना कोणतीही अडचण येणार नाही. चला सुरुवातीपासूनच ते मिळवूया.
काय समीकरण आहे
त्याद्वारे निवडलेल्या अभिकर्मकांमध्ये होणाऱ्या रासायनिक अभिक्रियाची सशर्त रेकॉर्ड असा अर्थ लावण्याची प्रथा आहे. अशा प्रक्रियेसाठी, निर्देशांक, गुणांक, सूत्रे वापरली जातात.
संकलन अल्गोरिदम
रासायनिक समीकरणे कशी लिहायची? मूळ संयुगे एकत्रित करून कोणत्याही परस्परसंवादाची उदाहरणे लिहिली जाऊ शकतात. समान चिन्ह हे सूचित करते की प्रतिक्रिया देणाऱ्या पदार्थांमध्ये परस्परसंवाद आहे. पुढे, व्हॅलेन्सी (ऑक्सिडेशन स्थिती) द्वारे उत्पादनांसाठी एक सूत्र संकलित केले आहे.
प्रतिक्रिया कशी नोंदवायची
उदाहरणार्थ, तुम्हाला मिथेनच्या गुणधर्मांची पुष्टी करणारी रासायनिक समीकरणे लिहायची असल्यास, खालील पर्याय निवडा:
- हॅलोजनेशन (डी. आय. मेंडेलीव्हच्या नियतकालिक सारणीच्या VIIA घटकासह मूलगामी परस्परसंवाद);
- वातावरणातील ऑक्सिजनमध्ये ज्वलन.
पहिल्या प्रकरणात, आम्ही डाव्या बाजूला प्रारंभिक पदार्थ आणि उजवीकडे परिणामी उत्पादने लिहितो. प्रत्येक रासायनिक घटकाच्या अणूंची संख्या तपासल्यानंतर, आम्ही चालू प्रक्रियेची अंतिम नोंद मिळवतो. जेव्हा वातावरणातील ऑक्सिजनमध्ये मिथेन जळते तेव्हा एक एक्झोथर्मिक प्रक्रिया उद्भवते, परिणामी कार्बन डायऑक्साइड आणि पाण्याची वाफ तयार होते.
रासायनिक समीकरणांमध्ये गुणांक योग्यरित्या ठेवण्यासाठी, पदार्थांच्या वस्तुमानाच्या संवर्धनाचा नियम वापरला जातो. आम्ही कार्बन अणूंची संख्या निर्धारित करून समायोजन प्रक्रिया सुरू करतो. पुढे, आम्ही हायड्रोजनची गणना करतो आणि त्यानंतरच आम्ही ऑक्सिजनचे प्रमाण तपासतो.
OVR
इलेक्ट्रॉनिक समतोल किंवा अर्ध-प्रतिक्रियांच्या पद्धतीचा वापर करून जटिल रासायनिक समीकरणे समान केली जाऊ शकतात. आम्ही खालील प्रकारच्या प्रतिक्रियांमध्ये गुणांक व्यवस्थित करण्यासाठी डिझाइन केलेल्या क्रियांचा क्रम ऑफर करतो:
- कुजणे;
- बदली

प्रथम, कंपाऊंडमधील प्रत्येक घटकाची ऑक्सिडेशन स्थिती व्यवस्थित करणे महत्वाचे आहे. त्यांना ठेवताना, काही नियम विचारात घेणे आवश्यक आहे:
- साध्या पदार्थासाठी ते शून्य असते.
- बायनरी कंपाऊंडमध्ये त्यांची बेरीज 0 असते.
- तीन किंवा अधिक घटकांच्या संयुगात, पहिल्याचे सकारात्मक मूल्य असते आणि शेवटच्या आयनमध्ये ऑक्सिडेशन स्थितीचे नकारात्मक मूल्य असते. मध्यवर्ती घटकाची बेरीज 0 असावी हे लक्षात घेऊन गणिती पद्धतीने मोजले जाते.
पुढे, ते अणू किंवा आयन निवडले जातात ज्यासाठी ऑक्सिडेशन स्थिती बदलली आहे. अधिक आणि वजा चिन्हे इलेक्ट्रॉनची संख्या दर्शवतात (स्वीकारलेले, दिलेले). पुढे, त्यांच्यामध्ये सर्वात लहान गुणाकार निर्धारित केला जातो. एनओसीला या आकड्यांद्वारे विभाजित केल्यावर क्रमांक मिळतात. हे अल्गोरिदम रासायनिक समीकरणांमध्ये गुणांक कसे व्यवस्थित करायचे या प्रश्नाचे उत्तर असेल.
पहिले उदाहरण
समजा कार्य दिले आहे: "प्रतिक्रियेतील गुणांक व्यवस्थित करा, अंतर भरा, ऑक्सिडायझिंग एजंट आणि कमी करणारे एजंट निश्चित करा." अशी उदाहरणे शालेय पदवीधरांना दिली जातात ज्यांनी त्यांची परीक्षा म्हणून रसायनशास्त्र निवडले आहे.
KMnO 4 + H 2 SO 4 + KBr = MnSO 4 + Br 2 +…+…

भविष्यातील अभियंते आणि चिकित्सकांना ऑफर केलेल्या रासायनिक समीकरणांमधील गुणांक कसे व्यवस्थित करावे हे समजून घेण्याचा प्रयत्न करूया. प्रारंभिक सामग्री आणि उपलब्ध उत्पादनांमधील घटकांच्या ऑक्सिडेशन स्थितीची मांडणी केल्यानंतर, आम्हाला आढळले की मॅंगनीज आयन ऑक्सिडायझिंग एजंट म्हणून कार्य करते आणि ब्रोमाइड आयन कमी करण्याचे गुणधर्म दर्शविते.
आम्ही असा निष्कर्ष काढतो की गहाळ पदार्थ रेडॉक्स प्रक्रियेत भाग घेत नाहीत. गहाळ उत्पादनांपैकी एक पाणी आहे, आणि दुसरे पोटॅशियम सल्फेट असेल. इलेक्ट्रॉनिक शिल्लक संकलित केल्यानंतर, समीकरणातील गुणांकांची सेटिंग ही अंतिम पायरी असेल.
दुसरे उदाहरण
रेडॉक्स प्रकाराच्या रासायनिक समीकरणांमध्ये गुणांक कसे व्यवस्थित करायचे हे समजून घेण्यासाठी दुसरे उदाहरण देऊ.
समजा आमच्याकडे खालील स्कीमा आहे:
P + HNO 3 \u003d NO 2 + ... + ...
फॉस्फरस, जो नियमानुसार एक साधा पदार्थ आहे, कमी करणारे गुणधर्म प्रदर्शित करतो, ऑक्सिडेशन स्थिती +5 पर्यंत वाढवतो. म्हणून, गहाळ पदार्थांपैकी एक फॉस्फोरिक ऍसिड H 3 PO 4 असेल. OVR कमी करणार्या एजंटची उपस्थिती गृहीत धरते, जे नायट्रोजन असेल. ते नायट्रिक ऑक्साईड (4) मध्ये जाते, NO 2 बनते

या अभिक्रियामध्ये गुणांक ठेवण्यासाठी, आम्ही इलेक्ट्रॉनिक शिल्लक बनवू.
P 0 परत देतो 5e = P +5
N +5 घेते e = N +4
नायट्रिक ऍसिड आणि नायट्रिक ऑक्साईड (4) 5 च्या घटकापूर्वी असणे आवश्यक आहे हे लक्षात घेता, आम्हाला पूर्ण प्रतिक्रिया मिळते:
P + 5HNO 3 \u003d 5NO 2 + H 2 O + H 3 PO 4
रसायनशास्त्रातील स्टिरिओकेमिकल गुणांक विविध संगणकीय समस्या सोडविण्यास अनुमती देतात.
तिसरे उदाहरण
गुणांकांची नियुक्ती अनेक हायस्कूल विद्यार्थ्यांना अडचणी निर्माण करते हे लक्षात घेता, विशिष्ट उदाहरणे वापरून क्रियांचा क्रम तयार करणे आवश्यक आहे. आम्ही कार्याचे आणखी एक उदाहरण देतो, ज्याच्या अंमलबजावणीसाठी रेडॉक्स प्रतिक्रियेतील गुणांक व्यवस्थित करण्याच्या पद्धतीवर प्रभुत्व असणे आवश्यक आहे.
H 2 S + HMnO 4 \u003d S + MnO 2 +…

प्रस्तावित कार्याची वैशिष्ठ्य अशी आहे की गहाळ प्रतिक्रिया उत्पादनास पूरक करणे आवश्यक आहे आणि त्यानंतरच आपण गुणांक सेट करण्यास पुढे जाऊ शकता.
यौगिकांमधील प्रत्येक घटकाच्या ऑक्सिडेशन स्थितीची मांडणी केल्यानंतर, असा निष्कर्ष काढला जाऊ शकतो की मॅंगनीज, जे व्हॅलेन्स कमी करते, ऑक्सिडायझिंग गुणधर्म प्रदर्शित करते. सल्फर प्रस्तावित प्रतिक्रियेमध्ये कमी करण्याची क्षमता दाखवते, एका साध्या पदार्थात कमी केले जाते. इलेक्ट्रॉनिक शिल्लक संकलित केल्यानंतर, आम्हाला केवळ प्रस्तावित प्रक्रिया योजनेमध्ये गुणांक ठेवावे लागतील. आणि कृत्य झाले आहे.
चौथे उदाहरण
रासायनिक समीकरणाला पूर्ण प्रक्रिया असे म्हणतात जेव्हा त्यात पदार्थांच्या वस्तुमानाच्या संवर्धनाचा नियम पूर्णपणे पाळला जातो. हा नमुना कसा तपासायचा? अभिक्रियामध्ये प्रवेश केलेल्या समान प्रकारच्या अणूंची संख्या परस्परसंवाद उत्पादनांमधील त्यांच्या संख्येशी संबंधित असणे आवश्यक आहे. केवळ या प्रकरणात रेकॉर्ड केलेल्या रासायनिक परस्परसंवादाची उपयुक्तता, गणनेसाठी त्याचा वापर करण्याची शक्यता, जटिलतेच्या विविध स्तरांच्या संगणकीय समस्या सोडवणे याबद्दल बोलणे शक्य होईल. येथे कार्याचा एक प्रकार आहे, ज्यामध्ये प्रतिक्रियेतील गहाळ स्टिरिओकेमिकल गुणांकांची व्यवस्था समाविष्ट आहे:
Si + ... + HF = H 2 SiF 6 + NO + ...

कार्याची जटिलता अशी आहे की प्रारंभिक पदार्थ आणि परस्परसंवादाची उत्पादने दोन्ही वगळण्यात आली आहेत. ऑक्सिडेशन स्थितीचे सर्व घटक सेट केल्यानंतर, आम्ही पाहतो की सिलिकॉन अणू प्रस्तावित कार्यामध्ये कमी गुणधर्म प्रदर्शित करतो. नायट्रोजन (II) प्रतिक्रिया उत्पादनांमध्ये उपस्थित आहे, सुरुवातीच्या संयुगांपैकी एक नायट्रिक ऍसिड आहे. तार्किकदृष्ट्या, आम्ही निर्धारित करतो की प्रतिक्रियेचे गहाळ उत्पादन पाणी आहे. अंतिम टप्पा प्रतिक्रिया मध्ये प्राप्त स्टिरिओकेमिकल गुणांकांची व्यवस्था असेल.
3Si + 4HNO 3 + 18HF = 3H 2 SiF 6 + 4NO + 8 H 2 O
समीकरण समस्येचे उदाहरण
हायड्रोजन क्लोराईडच्या 10% द्रावणाचे प्रमाण निश्चित करणे आवश्यक आहे, ज्याची घनता 1.05 ग्रॅम / एमएल आहे, त्याच्या कार्बाइडच्या हायड्रोलिसिस दरम्यान तयार झालेल्या कॅल्शियम हायड्रॉक्साईडच्या संपूर्ण तटस्थतेसाठी आवश्यक आहे. हे ज्ञात आहे की हायड्रोलिसिस दरम्यान सोडलेला वायू 8.96 लिटर (n.a.) ची मात्रा व्यापतो.
CaC 2 + 2H 2 O \u003d Ca (OH) 2 + C 2 H 2
कॅल्शियम हायड्रॉक्साईड हायड्रोजन क्लोराईडशी संवाद साधते, पूर्ण तटस्थीकरण होते:
Ca (OH) 2 + 2HCl \u003d CaCl 2 + 2H 2 O

आम्ही या प्रक्रियेसाठी आवश्यक असलेल्या आम्लाच्या वस्तुमानाची गणना करतो. हायड्रोजन क्लोराईड द्रावणाची मात्रा निश्चित करा. समस्येची सर्व गणना स्टिरिओकेमिकल गुणांक लक्षात घेऊन केली जाते, जे त्यांचे महत्त्व पुष्टी करते.
शेवटी
रसायनशास्त्रातील युनिफाइड स्टेट परीक्षेच्या निकालांचे विश्लेषण असे दर्शविते की समीकरणांमध्ये स्टिरिओकेमिकल गुणांक सेट करणे, इलेक्ट्रॉनिक शिल्लक संकलित करणे, ऑक्सिडायझिंग एजंट आणि कमी करणारे एजंट निश्चित करणे यासारख्या कार्यांमुळे माध्यमिक शाळांच्या आधुनिक पदवीधरांना गंभीर अडचणी येतात. दुर्दैवाने, आधुनिक पदवीधरांच्या स्वातंत्र्याची डिग्री व्यावहारिकदृष्ट्या कमी आहे, म्हणून हायस्कूलचे विद्यार्थी शिक्षकाने प्रस्तावित केलेल्या सैद्धांतिक आधारावर काम करत नाहीत.
विविध प्रकारच्या प्रतिक्रियांमध्ये गुणांक टाकताना शाळकरी मुले ज्या ठराविक चुका करतात, त्यात अनेक गणिती चुका आहेत. उदाहरणार्थ, किमान सामान्य गुणक कसे शोधायचे, भागाकार आणि गुणाकार योग्यरित्या कसा करायचा हे प्रत्येकाला माहित नाही. या घटनेचे कारण म्हणजे या विषयाच्या अभ्यासासाठी शैक्षणिक शाळांमध्ये वाटप केलेल्या तासांची संख्या कमी होणे. रसायनशास्त्रातील मूलभूत कार्यक्रमासह, शिक्षकांना त्यांच्या विद्यार्थ्यांच्या रेडॉक्स प्रक्रियेमध्ये इलेक्ट्रॉनिक शिल्लक संकलनाशी संबंधित समस्यांसह कार्य करण्याची संधी नसते.
